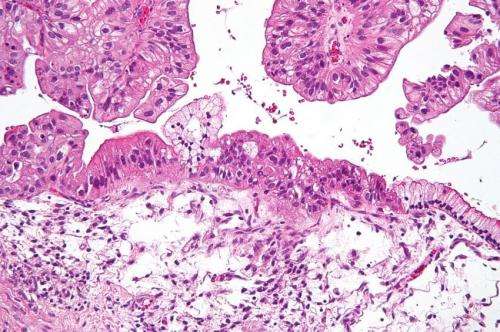
میکروگراف بزرگنمایی متوسط از یک تومور مخاطی تخمدان با پتانسیل بدخیم کم (LMP). لکه H&E. میکروگراف نشان می دهد: اپیتلیوم موسینوس ساده (راست) و اپیتلیوم موسینوز که شبه چینه می شود (سمت چپ – تشخیص تومور LMP). اپیتلیوم در معماری ورقه مانند در بالای تصویر دیده می شود. اعتبار: نفرون / ویکی پدیا. CC BY-SA 3.0
داده های به روز شده گسترش دوز فاز I مطالعه STRO-002-GM1 امروز توسط Ana Oaknin، محقق اصلی گروه بدخیمی های زنان در موسسه سرطان شناسی Vall d’Hebron (VHIO) در محل در نشست سالانه 2023 ارائه شده است. انجمن آمریکایی انکولوژی بالینی (ASCO)، 2-6 ژوئن در شیکاگو، ایالات متحده.
این مطالعه جهانی به منظور ارزیابی اثربخشی و ایمنی داروی مزدوج آنتیبادی هدفگیری FolRα (ADC) luveltamab tazevibulin (STRO-002-luvelta) در بیماران مبتلا به سرطان تخمدان اپیتلیال عودکننده با سطوح بیان مشخص شده گیرنده فولات آلفا (FolRα) طراحی شد. بالاتر از 25 درصد این ADC باعث مرگ سلولی سیتوتوکسیک و ایمونولوژیک و با استفاده از فناوری کونژوگاسیون مکان خاص می شود و برای هدف قرار دادن طیف وسیعی از تومورهای تخمدان بیان کننده FolRα طراحی شده است.
گیرنده فولات آلفا یک پروتئین متصل به فولات است که بیش از حد بر روی تخمدان و چندین بدخیمی دیگر اپیتلیال بیان می شود. بیان بیش از حد آن در تومورهای جامد باعث تکثیر سلول های سرطانی می شود و در بیماری متاستاتیک یا عود کننده پس از درمان ادامه می یابد. بنابراین این محرک تکثیر سلول های سرطانی یک هدف بسیار مرتبط است. برای توسعه استراتژی های درمانی جدید در سرطان های تخمدان و آندومتر.”
STRO-002-GM1 44 بیمار مبتلا به سرطان تخمدان پیشرفته و عود بیماری را در نتیجه مقاومت در برابر شیمی درمانی پلاتین پس از 1-3 خط قبلی درمان یا بیماری حساس به پلاتین بعد از 2-3 خط قبلی شیمی درمانی پلاتین وارد کرد. بیان FolRα برای ورود به مطالعه مورد نیاز نبود، اما به صورت گذشته نگر در بافت بایگانی مورد تجزیه و تحلیل قرار گرفت تا ارزیابی شود که آیا بیان بیش از حد این پروتئین می تواند به طور بالقوه انتخاب بیمار را هدایت کند.
بیماران 1:1 برای دریافت لوولتاماب با دوز 4.3 میلی گرم بر کیلوگرم یا 5.2 میلی گرم بر کیلوگرم (به ترتیب 23 بیمار و 21 بیمار) تصادفی شدند. 33 نفر از 44 بیمار ثبت نام شده در این مطالعه با سطوح بیان FolRα بالاتر از 25٪ مراجعه کردند. دادههای افزایش دوز، مزایای بالینی قابلتوجهی را در بیمارانی که برای ارائه بیان FolRα > 25 درصد انتخاب شدهاند، با نرخ پاسخ کلی 37.5 درصد نشان میدهد. محققان نرخ پاسخ 44 درصدی را در بیمارانی مشاهده کردند که درمان با دوز 5.2 میلی گرم بر کیلوگرم بالاتر را دریافت کردند.
شایع ترین عوارض جانبی شامل نوتروپنی، آرترالژی و کم خونی بود که با درمان استاندارد پزشکی و کاهش دوز کنترل شد. بروز نوتروپنی در mg/kg 2/5 بیشتر از mg/kg 3/4 بود. در حالی که عوارض جانبی درمان منجر به کاهش دوز در 76٪ از بیماران تحت درمان با دوز 5.2 میلی گرم بر کیلوگرم شد، درمان فقط در یک بیمار به حالت تعلیق درآمد.
این دادههای افزایش دوز، فعالیت تشویقکننده لوولتاماب تازوویبولین را در دوزهای شروع از 4.3 تا 5.2 میلیگرم بر کیلوگرم در بیماران مبتلا به سرطان تخمدان عودکننده مقاوم به پلاتین با سطح بیان FolRα بیش از 25 درصد تأیید میکند و از ارزیابی بالینی بیشتر حمایت میکند. محققین VHIO در اروپا، یک مطالعه جهانی فاز II/III قبلاً برای ارزیابی این ADC جدید در این جمعیت بیمار برنامه ریزی شده است.”
اطلاعات بیشتر:
کنفرانس:conferences.asco.org/am/attend
ارائه شده توسط موسسه انکولوژی Vall d’Hebron
نقل قول: داروی مزدوج آنتیبادی جدید FolRα در سرطان عودکننده اپیتلیال تخمدان نویدبخش است (2023، 3 ژوئن) بازیابی شده در 3 ژوئن 2023 از https://medicalxpress.com/news/2023-06-folr-targeting-antibody-drug-conjugate- مکرر.html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.