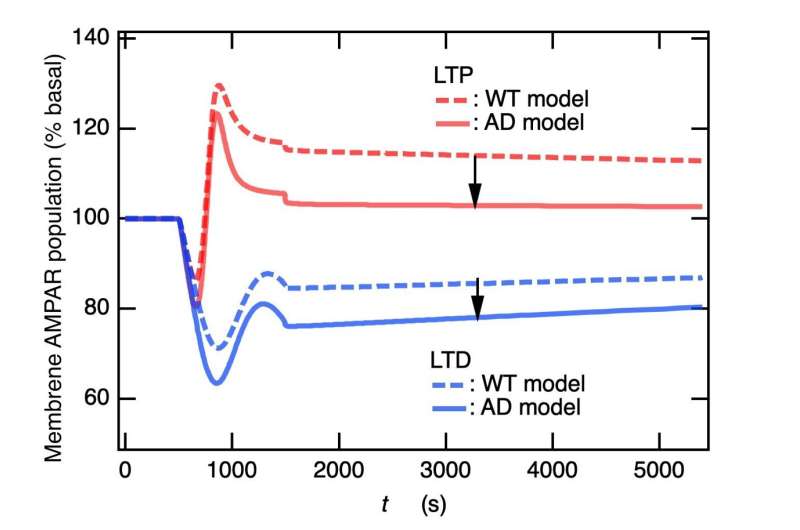
نمودار مشارکت درصد جمعیت AMPAR غشای پایه را در تقویت و تمایز طولانی مدت در مدل های حیوانی نوع وحشی و بیماری آلزایمر نشان می دهد. این مطالعه نشان می دهد که تقویت و تمایز طولانی مدت وابسته به M1-mAChR و NMDAR یک مسیر مشترک دارند. اعتبار: توموناری سومی و کوجی هارادا از دانشگاه اوکایاما
شواهد علمی نشان میدهد که چگونه کاهش شناختی در بیماری آلزایمر (AD) به دلیل تجمع پروتئینهای بتا آمیلوئید ایجاد میشود که باعث اختلال در عملکرد سیناپسی میشود. یکی از ویژگی های نوروپاتولوژیک در مغز بیماران مبتلا به AD، انحطاط نورون های کولینرژیک پایه پیش مغز است که منجر به کاهش تعداد برجستگی های کولینرژیک به هیپوکامپ می شود.
به عنوان یک درمان علامتی AD، انتقال عصبی کولینرژیک با استفاده از داروهای خاصی که به عنوان مهارکننده های استیل کولین استراز شناخته می شوند، افزایش می یابد. برای پیشگیری و درمان بهتر اختلالات شناختی مانند AD و اسکیزوفرنی، لازم است بدانیم که چگونه استیل کولین انتقالات سیناپسی را تنظیم می کند.
عملکردهای بالاتر مغز، مانند یادگیری و حافظه، تا حدی با ارسال سیگنال از طریق گیرنده استیل کولین موسکارینی M1 (mAChR) تنظیم می شود. mAChR همچنین باعث تقویت طولانی مدت (LTP) و افسردگی طولانی مدت (LTD) انتقال سیناپسی تحریکی در هیپوکامپ می شود. در طول فعالیتهای یادگیری تحت کنترل هیپوکامپ، سطوح خارج سلولی استیل کولین (Ach) 4 برابر در هیپوکامپ افزایش مییابد که توسط انتقال سیگنال mAChR هدایت میشود.
فعال سازی mAChR توسط آگونیست ها (مواد شیمیایی فعال کننده) برای القای LTP و LTD در هیپوکامپ شناخته شده است، اما مکانیسم های مولکولی زیربنایی به خوبی شناخته نشده است.
برای مطالعه این مکانیسمهای مولکولی، دانشمندان ژاپنی اخیراً مدلی برای ردیابی انعطافپذیری سیناپسی هیپوکامپ طراحی کردهاند. مطالعه آنها در منتشر شده است آی ساینس.
دانشیار توموناری سومی از دانشگاه اوکایاما، ژاپن، که این مطالعه را رهبری کرد، توضیح میدهد: «در اینجا، ما این فرضیه را پیشنهاد میکنیم که LTP و LTD وابسته به mAChR M1 گیرنده مشترک a-amino-3-hydroxy5-methyl-4-isoxazolepropionic acid را دارند. مسیر قاچاق (AMPAR) مرتبط با LTP و LTD وابسته به NMDAR.”
برای نورون های هیپوکامپ، یک مدل قاچاق گیرنده AMPA (AMPAR) برای شبیه سازی شکل پذیری سیناپسی وابسته به گیرنده N-متیل-D-آسپارتات (NMDAR) پیشنهاد شد. یافتههای این مطالعه اعتبار این فرضیه را اثبات میکند که LTP و LTD وابسته به mAChR یک مسیر قاچاق AMPAR مشترک دارند.
تفاوت بین این دو مسیر در این است که در فعال سازی M1-mAChR، Ca2+ یون های ذخیره شده در شبکه آندوپلاسمی نورون ها به سیتوزول ستون فقرات رها می شوند. رقابتی بین Ca2+ اگزوسیتوز و اندوسیتوز وابسته LTP و LPD را تنظیم می کند.
بنابراین، می توان نتیجه گرفت که القای وابسته به M1 mAChR LTP و LTD مسیر مشترک قاچاق AMPAR را با پلاستیسیته سیناپسی وابسته به NMDAR به اشتراک می گذارد و بیان ژن جدید حداقل در مراحل اولیه LTP و LTD ضروری نیست. کوجی هارادا از مرکز آموزش مبتنی بر فناوری اطلاعات، دانشگاه صنعتی تویوهاشی می گوید.
این یافته ها نشان می دهد که چگونه کاهش تعداد AMPAR ها به دلیل سطوح بیان ژن متفاوت بر القای LTP و LTD تأثیر می گذارد. این نتایج برای درک عوامل غالب منجر به تغییرات LTP و LTD در مدل های حیوانی AD مفید خواهد بود، که در نهایت می تواند برای توسعه درمان AD با هدف قرار دادن انعطاف پذیری سیناپسی برای انسان مفید باشد.
پیری مغز انسان باعث کاهش قابل توجهی در بیان تعدادی از گیرنده های انتقال دهنده عصبی مانند GluA1 می شود که باعث ادغام گیرنده های AMPA در داخل غشاهای سیناپسی می شود. مدل قاچاق AMPAR نشان می دهد که تغییرات در LTP و LTD مشاهده شده در AD می تواند به دلیل کاهش مربوط به سن در سطوح بیان AMPAR باشد.
دکتر سومی میگوید: «در مجموع، این مشاهدات نشان میدهند که تنظیم مثبت ژنهای گیرنده انتقالدهندههای عصبی یا سرکوب کاهش تنظیم میتواند اختلال عملکرد سیناپسی را در طول AD بهبود بخشد».
اطلاعات بیشتر:
Tomonari Sumi و همکاران، وابسته به گیرنده استیل کولین موسکارینی و LTP و LTD وابسته به گیرنده NMDA مسیر مشترک قاچاق AMPAR را دارند. آی ساینس (2023). DOI: 10.1016/j.isci.2023.106133
ارائه شده توسط دانشگاه اوکایاما
نقل قول: دانشمندان نشان میدهند که چگونه بیان ژن انعطافپذیری سیناپسی را در مغز انسان سالخورده کنترل میکند (2023، 8 مارس) بازیابی شده در 8 مارس 2023 از https://medicalxpress.com/news/2023-03-scientists-gene-synaptic-plasticity-aging.html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.